Für die Automatisierung der Festphasenextraktion stehen SPE-Kartuschenmodule zur Verfügung, die handelsübliche SPE-Kartuschen, Wasserextraktionsdisks, Flash-Kartuschen und Filter aufnehmen können. Nach der Festphasenextraktion kann die Probe eingeengt und ein Lösungsmittelwechsel durchgeführt werden.
Probenvorbereitungsplattform PrepLinc
PrepLinc - das modulare System für die vollautomatisierte Probenvorbereitung
Mit der PrepLinc-Plattform werden unzählige Probenreinigungsschritte vollständig automatisiert - und das reproduzierbar, verlustfrei und ohne Kreuzkontaminationen.
Das PrepLinc System wird u. a. für die Aufreinigung von Lebensmittelproben, Wasserproben, Futtermittelproben, Umweltproben, Kraftstoffen, pharmazeutischen Proben, Humanproben eingesetzt. Das System bietet die Möglichkeit, umfangreiche und arbeitsintensive Arbeitsschritte zu verknüpfen und komplett zu automatisieren - manuelle Zwischenschritte sind nicht mehr erforderlich.
Festphasenextraktion (SPE)
Bei der Festphasenextraktion handelt es sich, ähnlich wie bei der Säulenchromatografie, um einen physikalischen Extraktionsprozess, der zwischen einer festen und einer flüssigen Phase stattfindet. Die zu extrahierende Probe wird in der SPE-Kartusche angereichert und anschließend mit einem Lösemittel elutiert. Durch die hohe Anpassungsfähigkeit der PrepLinc an bestehende Methoden sowie der exakten Anpassung an bestehende Applikationsparameter werden auch komplexe Methoden mit der PrepLinc automatisiert. Durch die Integration der Probenkonzentration mit Lösemittelaustausch (AVM) und der Möglichkeit, Proben zwischen zwei Probenvorbreitungsschritten filtrieren zu können sind keine manuellen Zwischenschritte notwendig - die PrepLinc liefert injektionsbereite Proben und transferiert diese in Vials (z. B. GC-Vials).
Elutions-Modi
Die SPE-Kartuschen des PrepLinc-Systems können wie folgt eluiert werden:
| Elution von oben nach unten | |
| Reverse-Elution | |
| Bypass-Elution | |
| Elution über Probenschleife, Kartusche Inline | |
| Elution über Probenschleife, Kartusche im Bypass | |
| Elution ohne Probenschleife, Kartusche Inline | |
| Elution ohne Probenschleife, Kartusche im Bypass |
Folgende Schritte können mit dem SPE-Modul vollautomatisch abgearbeitet werden
- SPE: Konditionieren, Probenaufgabe, Verdünnen, Durchmischen, Waschen, Trocknen, Eluieren, Umkehreluieren, Fraktionieren, Spülen, Probentransfer
- Liquid Handling: Dosieren, Dispensieren, Verdünnen, Lösen, Transferieren, Pipettieren, Homogenisieren, Probenteilung, Systemreinigung
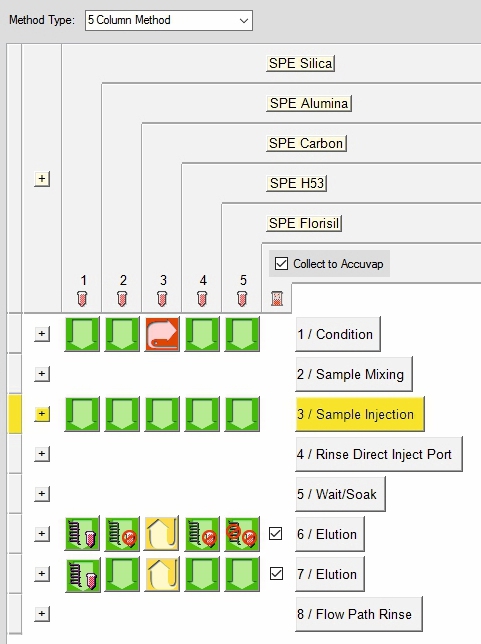
SPE Module
Für die Automatisierung der Festphasenextraktion stehen unterschiedliche SPE-Kartuschenmodule zur Verfügung, die handelsübliche SPE-Kartuschen, Wasserextraktionsdisks, Flash-Kartuschen und Filter aufnehmen können.
Es können Einfach- sowie Mehrfachkartuschenmethoden abgearbeitet werden. Die SPE-Kartuschenmodule können in beliebiger Reihenfolge mit anderen Probenvorbereitungsmodulen geschaltet werden. So können selbst hochkomplexe Aufarbeitungsmethoden auf der PrepLinc vollständig automatisiert werden.
SPE Modul SPEi

- Standardmodul zur Festphasenextraktion für handelsübliche SPE-KartuschenDie Probenaufgabe erfolgt über den SPE-Injektionsport oder inline von einem beliebigen PrepLinc-Modul.
Auf der PrepLinc-Plattform können bis zu fünf SPEi-Module mit jeweils neun SPE-Positionen eingesetzt werden.
Kartuschengröße: 1 ml bis 15 ml.
SPE-Methoden
- Folgende Schritte können mit dem SPE-Modul vollautomatisch abgearbeitet werden:
- SPE: Probenaufgabe, Konditionieren, Verdünnen, Waschen, Trocknen, Eluieren, Umkehreluieren, Fraktionieren, Spülen, Probentransfer
Liquid Handling: Dosieren, Dispensieren, Verdünnen, Lösen, Transferieren, Pipettieren, Homogenisieren, Probenteilung, Spülen, Probenaufgabe / Probenaufnahme
Merkmale des SPE-Moduls SPEi:
- Einsatz von Flashsäulen, Disks, Filter sowie von handelsübliche SPE-Kartuschen von 1 ml bis 15 ml
- bis zu 12 unterschiedliche Lösemittel können an das SPE Modul angeschlossen werden
- Multi-Säulen-Methoden
- Positiver Druck mit einstellbaren Durchflussraten
- Transfer direkt von beliebigen PrepLinc-Modul oder Direktinjektion möglich
- Reverse Flow bei jeder SPE-Kartusche möglich
SPE-Modul LVi

- Festphasenextraktionsmodul für großvolumige Proben mit LVi PumpenmodulDie Probenaufgabe erfolgt von einem beliebigen PrepLinc Modul inline oder über die LVi-Pumpe direkt aus dem Probenglas.
Auf der PrepLinc-Plattform können bis zu drei LVi-Module mit jeweils acht SPE-/Exktraktionsdisk-Positionen eingesetzt werden.
SPE-Methoden
- Folgende Schritte können mit dem SPE-Modul vollautomatisch abgearbeitet werden:
- SPE: Probenaufgabe, Konditionieren, Verdünnen, Waschen, Trocknen, Eluieren, Fraktionieren, Spülen, Probentransfer
Liquid Handling: Dosieren, Dispensieren, Verdünnen, Lösen, Transferieren, Pipettieren, Homogenisieren, Probenteilung, Spülen, Probenaufgabe / Probenaufnahme
Merkmale LVi Modul:
- geeignet für große Probenvolumina von 20 ml bis > 1 Liter
- speziell für Wasserextraktions-Disks entwickelt
- das LVi-Pumpenmodul gewährleistet eine konstante Flussrate bis zu 90 ml/min.
- handelsübliche Extraktions-Disks bis 50 mm Durchmesser und 100 mm Länge einsetzbar
- wählbare Flussrate für flussratenkritische Methoden
- automatische Anpassung des Durchflusses
- Druckwächter mit frei anpassbarem Abschaltdruck
- Kombination von mehreren Modulen (Multi-Säulen-Methode)
Automatisierung komplexer Methoden
PrepLinc automatisiert auch komplexe SPE-Anwendungen, bei denen mehrere SPE-Kartuschen Verwendung finden müssen. Das Applikationsbeispiel zeigt die Aufreinigung einer Dioxinprobe, die mit GPC, AccuVap und drei unterschiedlichen SPE-Kartuschen die PCBs, PBDEs und PCDD/Fs separiert. Die fertige, injektionsbereite Probe wird nach der vollautomatischen Probenaufreinigung vom PrepLinc System in Vials (z. B. GC Vials) abgefüllt.

Probenaufbereitung verschiedener Matrices für PCB, PCDD/F und PBDE Komponenten mit PrepLinc
Diese Probenaufbereitungen erfolgen durch GPC-Reinigung und mehrfachen SPE-Reinigungsschritten, wobei die Analyten durch Volumeneinengungen unter kontrolliertem Vakuum und Temperaturzufuhr im AccuVap Modul aufkonzentriert werden. Diese Aufkonzentrationen können auch mehrfach erfolgen, um ein oder auch mehrere Probenkonzentrate zur weiteren Analytik zu erhalten. Dies ist z. B. in dem nachfolgend beschriebenen Prozess der Fall, bei dem als Ergebnis je ein Vial mit den Analyten PCB/PBDE und PCDD/F gewonnen wird:
Das aus der GPC-Säule strömende Eluat wird, zeitlich um 20 Sekunden versetzt, sofort in der AccuVap-Kammer konzentriert. Dies wird durch Sensoren in der Verdampfungskammer überwacht und gesteuert. Nach Beendigung der GPC-Reinigung und der AccuVap-Konzentration wird das Eluat direkt aus der Verdampfungskammer der AccuVap über eine Kieselgel-Kartusche in SPE-Modul 1 und dann in SPE-Modul 2 über eine Aluminiumoxid-Kartusche in den Abfall geleitet.
Mit unterschiedlichen Lösemitteln erfolgen dann weitere Elutionen über die Kieselgel- und Aluminiumoxid-Kartusche sowie über die Kohlenstoff-Kartusche, um dann die PCB/PBDE-Analyten, nach weiterer Aufkonzentrierung in dem AccuVap Modul, in Probenvial 1 zu sammeln. Nun erfolgt eine Elution in umgekehrter Flussrichtung an der Kohlenstoff-Kartusche, um, wieder nach Konzentration in der AccuVap, die PCDD/F-Analyten in Vial 2 aufzunehmen. Mit dem Linc-Editor werden die drei Probenvorbereitungsmethoden, den einzelnen Modulen zugeordnet, zu einer Gesamtmethode vernetzt.
Umsetzung der Methode mit dem PrepLinc System
PrepLinc ist weltweit das einzige System, das die vorstehend geschilderte Methode vollautomatisiert durchführen kann. Die PrepLinc-Plattform wird mit den verfügbaren Hardware-Komponenten PrepLinc-GPC, PrepLinc-AccuVap und mit bis zu fünf PrepLinc-SPE-Modulen, die jeweils 9 handelsübliche SPE-Kartuschen aufnehmen können, bestückt. Mit der PrepLinc-Software werden diese Module in beliebiger Reihenfolge miteinander vernetzt, so dass damit die unterschiedlichsten Anforderungen realisiert werden. Höchstmögliche Flexibilität des PrepLinc-Systems ist damit gegeben. Der gesamte Ablauf geschieht vollautomatisiert vom Extrakt zu den zwei fertig abgefüllten GC-Vials, ohne dass manuelle Zwischenarbeiten erforderlich wären.

Probenkonzentration mit Lösemittelaustausch
Die Module zur Festphasenextraktion (SPE) und Gelpermeationschromatografie (GPC) erfahren in der Kombination mit dem Probenkonzentrationsmodul mit Lösemittelaustausch (AVM) einen weiteren Automatisierungseffekt. Das Konzentrationsmodul kann Inline angesteuert werden; die Proben werden direkt in die Verdampfungskammer geleitet und aufkonzentriert. In Verbindung mit dem GPC Modul geschieht dies meist während der Collect-Phase, beim SPE-Modul während der Elutions-Phase. Proben können auch in Vials in den Autosampler gestellt werden und werden in die AccuVap überführt und eingeengt. Ein besonderer Vorteil der AccuVap besteht darin, dass das Modul beliebig vor oder nach einem Probenvorbereitungsschritt geschaltet werden kann.
So können auch Methoden, die hohe Anforderungen an die Probenaufbereitung stellen, mit der PrepLinc Plattform vollumfänglich umgesetzt werden.
AccuVap Modul (AVM)
In der Rückstandsanalytik erfolgen nach der Probenaufreinigung mit GPC noch eine Reihe von manuellen Arbeitsschritten, bis die Proben zur endgültigen Untersuchung im GC/MS bereitstehen. Während die GPC Probenaufreinigung seit Jahren weitgehend automatisiert abläuft, wird die dann folgende Einengung der Wirkstoffe, der Lösemittelaustausch und das Abfüllen der Proben in GC Probengläschen noch oft von Hand erledigt. Auch der Einsatz halbautomatischer Verdampfungssysteme kann diese Arbeitsschritte nur teilweise ersetzen.
Um diese manuellen Arbeitsschritte völlig einsparen zu können und gleichzeitig die Laufzeiten von der Probenaufgabe am GPC bis zur Bereitstellung der Proben am GC drastisch zu verkürzen wurde das Verdampfungsmodul AVM entwickelt.
Das Evaporations-Modul AVM bietet einzigartige Möglichkeiten für die Probenvorbereitung und zeichnet sich durch folgende Eigenschaften aus:
- die Lösemittelverdampfung erfolgt beim Verdampfungsmodul unmittelbar nach dem Verlassen der Gelsäule in gleicher Menge, die der Flussrate des Eluenten im GPC bzw. SPE entspricht.
- der Verdampfungsvorgang erfolgt schonend ohne Siedeverzug. Dadurch werden Wirkstoffverluste vermieden und zugleich gewährleistet, dass sowohl ein Überlaufen als auch ein Trockenlaufen der Verdampfungskammer während der Einengung ausgeschlossen ist.
- das System ist in der Lage, bis zur Trockene einzuengen. Die nachfolgende Zugabe eines Austauschlösemittels, dessen Menge die Konzentration bestimmt, erfolgt sehr exakt.
- der Probentransfer in Vials erfolgt nahezu vollständig, auch bei kleinsten Probemengen steht ausreichend Material zur weiteren Verarbeitung zur Verfügung.
- Vakuum- und Heizraten werden abhängig vom Probenstand in der Kammer vom Gerät automatisch angepasst.
- Proben können gesplittet in unterschiedlichen Lösemitteln und in unterschiedliche Vials überführt werden.
- Sicherheitseinrichtungen gewährleisten einen Betrieb auch während der Nachtstunden und über das Wochenende.
- alle gemeinsam genutzten Wege werden so gespült, dass keinerlei Verschleppungen von einer Probe zur nächsten erfolgt.
- Das Endvolumen kann auf ein beliebiges Volumen eingeengt werden, das eingestellte Volumen ist durch das Geräteprogramm kalibrierbar.
- Das gewünschte Endvolumen kann von Probe zu Probe individuell in 1µl-Schritten vorgegeben werden.
- Einengung wahlweise schonend bis zur Trockene oder Einengung zum Level-Sensor (Flüssig/Flüssig) auch in einer Probensequenz.
Das AVM Inline-Verdampfungsmodul bietet darüber hinaus eine Reihe weiterer Möglichkeiten wie z.B. die wahlweise Wirkstoffeinengung zur Trockene oder mit mehrfachem Lösemittelaustausch, ohne zur Trockene zu gehen. Bei der AccuVap sind beide Verfahren möglich. Die Aufnahme der Wirkstoffe im Austauschlösemittel und der daran anschließende Transfer der Wirkstoffkonzentrate in GC-Vials kann mehrfach erfolgen. Die transferierten Mengen können frei gewählt werden. Vier unterschiedliche Austauschlösemittel können gleichzeitig am System angeschlossen sein und verwendet werden.
Modul für die Inline-Wirkstoffkonzentration und Lösemittelaustausch

- Extrakte oder Eluate werden der AccuVap in "kleinen Portionen" kontinuierlich zugeführt und dort entsprechend der Zuführmenge mit Vakuum und Temperatur, entweder schonend zur Trockene oder bis zu einem Flüssigkeitssensor eingedampft.
Die Trockene wird erst ganz am Schluss erreicht, wenn keine Probe der AccuVap mehr zugeführt wird. - Ein Lösungsmittelaustausch erfolgt, wenn erforderlich, ebenso wie der Transfer in GC- oder andere Vials, automatisch
- Besonderheiten des AccuVap-Moduls:
- - Vollautomatisiertes Probenkonzentrationssystem mit Lösemittelaustausch
- - Probenkonzentration vom SPE-Modul, GPC-Modul oder direkt aus einem Probenglas
- - Probenhomogenisierung vor dem Transfer
- - Schonende Einengung zur Trockene oder bis zu einem definierten Endvolumen (0,5 ml bis 10 ml, stufenlos)
- - Keine Siedeverzögerung durch intelligentes, statisches Verdampfungssystem, keine rotierenden Teile.
Keine Siedeverzögerung durch intelligentes, statisches Verdampfungssystem
"Trockene oder Restvolumen?"
AccuVap bietet beide Verdampfungsoptionen serienmäßig
Einengung zur Trockene
Die meisten Anwender engen zur Trockene ein. Das geschieht in der AccuVap sehr schonend und erst am Ende des Einengungsprozesses: Während der Verdampfung, die parallel zur Aufreinigung in der Gelsäule erfolgt, sind die Verdampfungstemperaturen entsprechend dem eingestellten Vakuum gleichbleibend niedrig. Am Endpunkt erkennt das System sofort, wenn die Trockene erreicht ist und schaltet augenblicklich den beheizten Boden der Verdampfungskammer ab, der zusätzlich mit einem Luft- oder Stickstoffstrom gekühlt wird. Durch die geringe Masse des beheizten Bodens wird die Temperatur-Hysterese extrem klein gehalten, so dass keine Wirkstoffverluste zu befürchten sind.
Einengung auf ein Restvolumen (Level Sensor)
Bei Einengung auf ein Restvolumen mit Lösungsmittelaustausch wird die Energiezufuhr zur Bodenheizung abgeschaltet, wenn der untere Sensor, der die Verdampfungskammer überwacht, erreicht wird. Es wird automatisch Austauschlösungsmittel zugegeben und es wird wieder zum unteren Sensor verdampft. Dies kann mehrmals erfolgen, so dass das nicht gewünschte Lösungsmittel mit Sicherheit verdampft ist. Um die immer gleiche Probenmenge zu transferieren, wird zum unteren Sensor automatisch aufgefüllt. Die Höhe des Sensors und damit die Probenmenge ist stufenlos einstellbar.
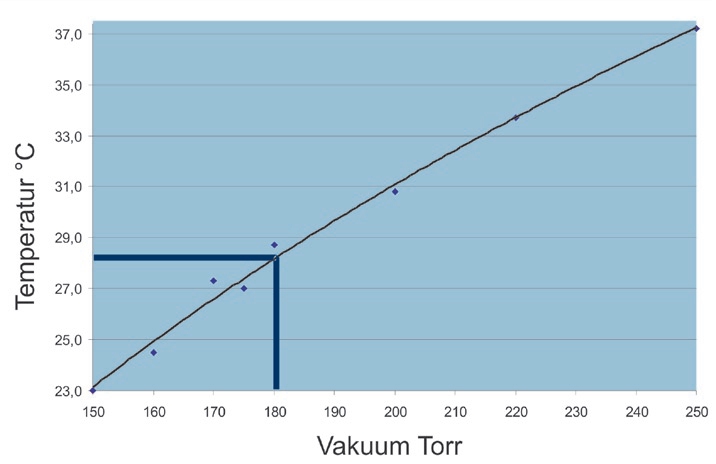
Temperatur-Verlauf
Temperaturverlauf bei unterschiedlichem Vakuum
Lösemittel: Ethylacetat : Cyclohexan 1:1
Vorzugsweise wird bei einem Vakuum von 180 Torr (=240 mbar) eingeengt, woraus sich eine Verdampfungstemperatur von etwa 28°C ergibt.
Hochpräzise Bauteile garantieren eine verlustfreie Probenkonzentration
Sensoren steuern automatisch die Temperatur- und Vakuumeinstellungen entsprechend dem Füllstand in der Verdampfungskammer und dem Arbeitsfortschritt. Der Level Sensor der Verdampfungskammer erkennt auch "schwierige" Proben - so lassen sich z. B. auch Kakaoproben problemlos konzentrieren. Die kleine Hysterese der Temperatur- und Vakuumsteuerung und die damit verbundene schonende Behandlung der Wirkstoffe ermöglicht die risikolose Einengung bis zur Trockene.
Lösemittelaustausch
Über ein automatisches Spritzenmodul erfolgt anschließend eine äußerst exakte Zugabe des Austauschlösemittels, mit der die Konzentration bestimmt wird. Zusätzlich bietet das Gerät die Alternative, den Lösemittelaustausch durch mehrmaliges Rückführen des Austauschlösemittels auf ein Restvolumen vorzunehmen. Zusätzlich läßt sich das System mit SPE Modulen aufrüsten und bietet so die Möglichkeit, einen weiteren Probenvorbereitungsschritt zu automatisieren.
FAQ
Das AccuVap Modul kann (entweder) sowohl Inline mit dem GPC- (bzw.) und/oder SPE-Modul als auch als Stand-alone-Verdampfungssystem verwendet werden.
In der Collect-Phase (GPC) bzw. Elutionsphase (SPE) wird die Probe direkt in das AccuVap-Modul überführt und dort unmittelbar "inline" eingeengt.
Bedingt durch die geniale Konstruktion der AccuVap-Verdampfungskammer erfolgt der Start des Einengungsprozesses unmittelbar nach Einleitung der ersten Milliliter des Eluates in der GPC-Collect-Phase bzw. in der SPE-Elutionsphase. D.b., dass die Probe nicht "zwischengelagert" werden muss, sondern parallel, zeitgleich zur Elution, in der AccuVap weiterverarbeitet wird.
Bei Verwendung der AccuVap als Stand-alone-Verdampfungssystem wird die Probe kontinuierlich aus Probengefäßen (z.B. Spitzkolben) durch Sensoren gesteuert entnommen, bis sich keine Flüssigkeit mehr im Vorlagegefäß befindet. Mit einem optionalen Spülvorgang des Vorlagegefäßes wird die vollständige Überführung auch eventueller Probenreste sicher gestellt.
In den Labor-Rotationsverdampfern wird der Verdampferkolben in einem Heizbad erwärmt und die Siedetemperatur durch Vakuum so abgesenkt dass auch temperaturempfindliche Substanzen weitgehend verlustfrei eingeengt werden. Solange sich Lösemittel im Verdampfungskolben befindet, bleibt die Verdampfungstemperatur gleichbleibend niedrig. Das ändert sich jedoch, wenn das Lösemittel im Verdampferkolben verdampft ist; dann steigt die Temperatur im Kolben schlagartig bis zur Temperatur des Heizbades. Durch die große Masse des Heizbades bedingt, läßt sich eine Temperaturabsenkung im Rotationsverdampfer nur sehr langsam erreichen. D.h., dass die Probe dem Heizbad entnommen werden muss, solange sich noch eine Restmenge Lösemittel im Kolben befindet. Eine ständige Überwachung der Restmenge im Verdampfungskolben ist also nötig, um diesen noch vor dem Erreichen der Trockene aus dem Heizbad zu entnehmen und damit die Zerstörung temperaturempfindlicher Substanzen zu verhindern.
Anders in der innovativen Verdampfungskammer der AccuVap: Auch hier wird die Verdampfungstemperatur durch Vakuum abgesenkt; der Verdampfungsvorgang erfolgt schonend ohne Siedeverzug. Durch die sehr geringe Masse des elekrisch beheizten Verdampfungskammer-Bodens wird die Temperatur des Bodens nach Abschaltung der elektrischen Heizenergie (beim Erreichen der Trockene, die elektronisch festgestellt wird) sehr schnell auf die Verdampfungstemperatur des Lösemittels abgesenkt. Die Temperaturhystere innerhalb der Kammer ist dadurch äußerst gering; auch temperaturempfindliche Substanzen können so verlustfrei zur Trockene gebracht werden.
Alternativ kann aber auch zu einem Restvolumen eingeengt und der Lösemittelaustausch mit einem höher siedenden Lösemittel durchgeführt werden.
Die Verdampfungskammer ist durch Sensoren in unterschiedliche Zonen aufgeteilt. In der unteren Zone wird der Kammerboden nicht beheizt und damit bleibt Lösemittel (ca. 0,5 bis 1 ml) in dieser Zone stehen. Die Wirkstoffe werden in diesem Lösemittelrest konzentriert und gehalten. Erst am Endpunkt (Ende der GPC-Collect-Phase, SPE-Elutions-Phase) ist in der Methode festgelegt, ob die Probe weiterhin zur Trockene oder zu einem Restvolumen eingeengt wird.
Die Temperatur in der Probe ist abhängig vom Lösemittel(gemisch) und vom angelegten Vakuum.
Bei Cyclohexan:Ethylacetat 1:1 und einem angelegtem Vakuum von 180 Torr ergibt sich eine Probentemperatur bei der Verdampfung von ca. 28°C.
Die Verdampfungskammer wird durch Sensoren in unterschiedliche Zonen unterteilt, damit sowohl ein Überlaufen als auch ein Trockenlaufen der Verdampfungskammer während der Einengung ausgeschlossen ist.
Ja. Der AccuVap-Sensor ist empfindlich gegenüber allen flüssigen Proben, unabhängig von der Probenkonzentration, der Probenmatrix oder vom Lösemittel in dem die Probe gelöst ist.
Auch "schwierige" Proben wie etwa Kakaoproben werden vom AccuVap-Sensor problemlos detektiert.
Für nachfolgende Analysensysteme (z. B. GC-MS/MS und LC-MS/MS) oder für weitere nachfolgende Probenaufreinigungsschritte (z. B. SPE) werden die Proben oft in unterschiedlichen Lösemitteln benötigt. Mit der AccuVap ist ein Split der Probe in unterschiedliche Konzentrationen und unterschiedlichen Lösemitteln möglich. Die Probe kann gesplittet und mit bis zu fünf unterschiedlichen Lösemitteln versetzt und dann transferiert (Vials, SPE-Modul, GPC-Modul) werden.
Autosampler mit Liquid Handling Modul
Das Liquid Handling Modul wird auf dem Autosampler platziert und bildet die Basis für jedes PrepLinc-Gerät. Das Grundgerät kann problemlos und jederzeit erweitert werden. Dafür stehen verschiedene Probenvorbereitungsmodule zur Verfügung.
Die Größe des Autosamplers bestimmt die Gesamtgröße der PrepLinc Plattform. Der Probengeber wird in zwei Größen angeboten: der AS2 mit einer Länge von 460 mm und der AS4 mit einer Länge von 805 mm.
Autosampler
Kapazität
Die PrepLinc mit einem Probengeber AS2 kann mit einem GPC Modul, einem AccuVap Modul und zwei SPE Module (entspricht 18 SPE-Kartuschen) ausgestattet werden. Die Kapazität kann mit einem Autosampler AS4 erhöht werden: bis zu fünf SPE Module können verwendet werden, dies entspricht 45 SPE-Kartuschen.
Nadelwaschstation
Es stehen unterschiedliche Waschstationen für das Autosampler-Modul zur Verfügung. Zur Reinigung der Nadel wird diese in die Nadelwaschstation gefahren und von innen wie von außen gereinigt.
Fällt bei der Probenaufreinigung Abwasser an, so wird dieses getrennt vom Lösemittelabfall in eine separate Flasche entleert um Entsorgungskosten zu minimieren.
Probenracks
Für den Autosampler stehen mehr als 50 Standard-Probentische (Racks) in unterschiedlichen Größen zur Auswahl.
Auch vorhandene oder selbstangefertigte Probentische können im Programm angelegt und verwendet werden.
Höchste Flexibilität - einfaches Handling
Die Racks werden beliebig auf dem nummerierten Lochraster der Grundplatte eingerastet. Der Lochrasterpunkt für jedes platzierte Rack wird in der Probentischkonfiguration (Mat-Editor) festgelegt.
Die Methoden werden rackunabhängig abgespeichert - Gerätekonfiguration, Mat-Editor und Methoden können beliebig miteinander kombiniert werden. Höchstmögliche Flexibilität ist dadurch gegeben.
Zehn unterschiedliche Nadeltiefen - pro Rack
Im Programm können bis zu zehn unterschiedliche Nadeltiefen pro Rack vom Anwender definiert werden, die dann bei der vollautomatischen Probenaufreinigung vom System berücksichtigt werden.
Liquid Handling Modul
An das Liquid Handling Modul können unterschiedliche Lösemittel angeschlossen werden. Durch hochpräzise Mikroliterspritzen und die Möglichkeit, die Spritzengeschwindigkeit an die Lösemittel und Methoden anzupassen, wird größtmögliche Präzision und Genauigkeit erzielt.
Folgende Schritte können durch das Liquid Handling Modul der PrepLinc-Plattform automatisiert werden, wodurch manuelle Zwischenschritte verhindert werden.
12+3 unterschiedliche Lösemittel
Neben den 12 unterschiedlichen Lösemitteln am SPE-Modul stehen dem Anwender drei weitere Lösemittel, die am Autosampler-Modul angeschlossen werden können, zur Verfügung.
So können sämtliche Applikationen auf der Probenvorbereitungsplattform automatisiert und ausgeführt werden - ohne Umbaumaßnahmen, auch in einer Sequenz.
Probenvorbereitungsmodule hinzufügen: Plug & Play
Weitere Module für die Probenaufreinigung können dem PrepLinc-System jederzeit und einfach hinzugefügt werden - es bedarf dazu keiner Umbauarbeiten.
Die Zusatzmodule werden mit einem Netzwerkkabel verbunden und damit im Programm registriert. Sofort stehen diese dann dem Anwender zur Verfügung.
Downloads
Anwendungsdatenblätter



Veröffentlichung von Dr. Jérôme Kaiser, Nadine Hollmann, Helge W. Arz, Leibniz-Institut für Ostseeforschung Warnemünde (IOW), 18119 Rostock-Warnemünde im Journal of Chromatography A.
Lizensiert unter Creative Commons Attribution (CC BY 4.0).
Automated solid phase extraction of environmental lipid biomarkers
Der Artikel untersucht die Leistungsfähigkeit einer automatisierten Festphasenextraktion (aSPE) mittels der PrepLinc-Plattform (J2 Scientific) im Vergleich zur traditionellen manuellen SPE (mSPE) bei der Auftrennung von lipidhaltigen Biomarkern aus marinen Sedimenten. Diese Biomarker dienen der Rekonstruktion von Umwelt- und Klimaveränderungen.
Sowohl die aSPE- als auch die mSPE-Methode erzielten quantitativ ähnliche Ergebnisse in der Bestimmung charakteristischer Lipidfraktionen (n-Alkane, Alkenone, GDGTs), sodass beide Verfahren grundsätzlich austauschbar sind. Dennoch zeigten sich systematische Unterschiede in einigen Bereichen:
- Rückgewinnungsrate: Die aSPE erreichte im Mittel eine Wiederfindung von etwa 97 %, während mSPE bei 79 % lag. Die höhere Präzision der aSPE resultiert aus dem konstanten Druck- und Flussregime des automatisierten Systems.
- Lösungsmittelverbrauch: Die aSPE benötigt rund 3,5-mal mehr Lösungsmittel (ca. 90 mL/Sample gegenüber 25 mL bei mSPE), hauptsächlich für Spülvorgänge. Trotz der höheren Verbrauchsmenge ist das System durch sein geschlossenes Lösungsmittelkreislaufsystem wesentlich sicherer für das Laborpersonal und reduziert die Belastung durch Schadstoffe.
- Zeit- und Prozessvorteile: Die PrepLinc-Plattform kann bis zu 27 Proben in einem Lauf vollständig automatisiert verarbeiten, auch außerhalb der Arbeitszeiten. Sie spart somit erhebliche Laborzeit und benötigt keinen Abzug, da sie in einem geschlossenen System arbeitet.
- Analytische Genauigkeit: Unterschiede zwischen den Methoden traten v. a. bei den Alkenonen C38:2Et und C39:2Et auf, bedingt durch Koelutionen mit sterolbasierten Ethern. Hier ist Vorsicht geboten, da sich diese Unterschiede auf Temperatur- oder Salinitätsindizes auswirken können.
- Indizes und Proxys: Die wichtigsten biomarkerbasierten Parameter (z. B. UK’37, BIT, TEXH86) zeigten bei beiden Methoden nahezu identische Werte und hohe Reproduzierbarkeit (<10 % Fehler).
Fazit:
Die automatisierte SPE mit der PrepLinc-Plattform bietet eine reproduzierbare, sichere und zeitsparende Alternative zur manuellen SPE bei der Analyse von Umweltlipiden. Obwohl der Lösungsmittelverbrauch zunächst höher ist, kompensieren Automatisierungsgrad, Geschlossenheit des Systems und Langzeiteffizienz diesen Nachteil. Für großangelegte Studien, etwa in der Paläoklimaforschung, kann durch parallele Anwendung von aSPE und mSPE die Probenverarbeitung signifikant beschleunigt werden.
Anwendungsdatenblatt 75
Die Methode L00.00-34, Untersuchung von Lebensmitteln, Modulare Multimethode zur Bestimmung von Pflanzenschutzrückständen in Lebensmitteln (Erweiterte Neufassung der DFG-Methode S 19), Bausteine C1 (GPC) und C2 (SPE) wird mit der Probenvorbereitungsplattform PrepLinc vollständig automatisiert.
Die Extraktlösung aus einem der Bausteine E (L00.00-34) wird in einem 10 ml Glas in den Probengeber eingestellt. Die an das PrepLinc System angeschlossene GPC-Säule wird vor dem ersten Probelauf mit Cyclohexan:Ethylacetat 1:1 equilibriert. Das SPE-Modul wird mit einer Kieselgelsäule bestückt. Als Auffanggefäße für die Elutionen 0 bis 5 (Baustein C1) bzw. Elutionen 1 bis 5 (Baustein C2) werden GC vials in den Tray eingestellt. Über den Sequenz-Editor wird die Linc-Methode L00.00-34-GPC-SPE geladen und die Ein- und Ausgabevials bestimmt. Anschließend wird das Gerät gestartet, die Probe wird vollautomatisch gereinigt, eingeengt und nach einem Lösemittelaustausch in GC Vials abgefüllt.
Bitte fordern Sie bei Interesse das Anwendungsdatenblatt bei ANTEC GmbH an.
Anwendungsdatenblatt 132
Currently, 12 substances are regulated by the Stockholm Convention on Persistent Organic Pollutants (POPs) signed in May 2001 by 127 countries, and the work on finding new candidate chemicals to the convention has started. One group of substances in focus is polycyclic aromatic hydrocarbons (PAHs). They are formed during all types of incomplete combustion of organic matter, and they exhibit the characteristic POPs properties: persistence, bio-accumulation, adverse effects and potential for long-range environmental transportation to a certain extent. Many of the PAHs are carcinogenic, they are also believed to exhibit reproductive effects, as well as immune system inhibiting properties, genotoxicity and mutagenicity.
The development of innovative analytical methods for determination of PAHs has been and is of fundamental importance, due to the high carcinogenicity of these compounds. The quali-quantitative analysis of PAHs is an important challenge due to the low concentration at which these hydrocarbons may be present.
Bitte fordern Sie bei Interesse das Anwendungsdatenblatt bei ANTEC GmbH an.
Anwendungsdatenblatt 131
The use of Dietary Supplements by consumers has grown from <10% of the population to ~50% of the population over 10 years (US). Ginseng, one of the most popular botanical supplements, is a root crop requiring 4-7 years to mature. The long growing period increase the risk of fungal and insect attack. Numerous chlorinated pesticides, namely PCNB (Quintozene) and Tricyclazole are frequently found in ginseng samples. FDA & private laboratory testing revealed major contamination problems in the 1990’s which still persist today making residue monitoring a high priority. While many supplements can be routinely tested using modern techniques (QuEChERS), many chlorinated residues and high-lipid/saponin matrices can create challenges for this modern technique. Florisil column clean up (SPE) and Gel Permeation Chromatography (GPC) are utilized for such matrices. Historical GPC involved significant time and resources from the analyst to collect fractions, evaporate them and perform various solvent exchanges & SPE. Using the new-generation PrepLinc™ system, these functions are fully automated creating a ready-to-inject sample in an autosampler vial making GPC viable again for production laboratories. This poster (the first in a series) will introduce the system and briefly outline the methods utilized for sample preparation & provide matrix examples. Future posters/papers will provide further detail on the project.
Bitte fordern Sie bei Interesse das Anwendungsdatenblatt bei ANTEC GmbH an.
Anwendungsdatenblatt 120
Extract purification for pico- or nanogram scale GC/MS is time consuming, laborious and costly, and may suffer from performance variations in manual cleanup chromatography. Size exclusion (GPC) followed by adsorptive chromatography is useful for cleanup of biota, soil and sediment extracts for high resolution PCDD/PCDF analyses. GPC cleanup of extracts is allowed or encouraged in several EPA methods and is of great value to laboratories practicing such analyses. Sample extract cleanup for PCDD./PCDF always involve a carbon column stage. Sample concentrate, typically after other cleanups, is passed onto carbon and forward elution drives out various interferences. Reverse elution utilizes solvent containing a component (e.g. toluene) having great affinity for carbon. This disgorges PCDD/PCDF congeners into an eluate ready for evaporation and analysis.
In this study GPC eluate was forward eluted through a carbon cartridge (bed of powder mixed with granular substrate, packed between two frits) placed in line after the GPC column. During forward elution, target compounds collect at or near the column head while interferences are flushed forward. Valve switching enables reverse elution with toluene for collection of targets. Thus PCDD/PCDF sample cleanup can be conducted in highly automated fashion with minimal operator contact.
Bitte fordern Sie bei Interesse das Anwendungsdatenblatt bei ANTEC GmbH an.
Anwendungsdatenblatt 30
Chlorination of drinking water has been a commonly practiced method of disinfection for over a century. However, the disinfection by-products arising from the reaction of organic material in the water and chlorine may give rise to certain aberrant carcinogenic effects. EPA Method 552.1 and 552.3 prescribe procedures for testing of haloacid constituents in drinking water by ion-exchange or micro extraction, followed by esterification and quantitation by GC-ECD.
In this study, the 552.1 ion-exchange method is automated for different water samples to afford increased reproducibility, unattended operation, and consistency of sample loading and elution.
Bitte fordern Sie bei Interesse das Anwendungsdatenblatt bei ANTEC GmbH an.
- Bestimmung von leichten und schweren polycyclischen aromatischen Kohlenwasserstoffen (PAKs) in Fetten und Ölen pflanzlicher und tierischer Herkunft mittels automatisierter 2D-GPC und anschließender GC-MS-Detektion
- Automatisierte Probenvorbereitung für die Bestimmung von Pestizidrückständen in hocheffizienten Laboratorien mit GPC-GC-MS/MS und -LC-MS/MS
- Maximierte Probenaufgabe mit zweidimensionaler Gelpermeationschromatografie (2D-GPC)
- Automatisierung der Bausteine GPC, C1 und C2 der Methode L 00.00-34
- Maximizing Lipid Load With 2-Dimensional GPC Cleanup
- QuEChERS, SPE and GPC: A Comparison of Sample Preparation Techniques for Analysis of Pesticides in Problematic Matrices
- Automated GPC with Inline SPE to Improve Sample Cleanup Without Adding Time or Solvent
- Additional cleanup for DIN EN 12393 minimising matrix effects and improving result quality in GC-MS
- A Combined SPE Method for Analysis of Chloroacetic Acids in Drinking Water
- Cleanup-Methode für Nahrungsergänzungsmittel wie z.B. Ginseng
- Modifizierte Cleanup-Methode für Dioxine und persistente organische Schadstoffe (POPs)
- Automatisierung der Wasserextraktion mit dem SPE-Wasserextraktionssystem LVi
- Traditionelles Dioxin-Cleanup mit dem PrepLinc System
- Wiederauffindungsraten unterschiedlicher Pflanzenschutzmittel mit GPC und AccuVap
- Erfahrungen zur Automatisierung des GPC-Reinigungsver fahrens bei der Untersuchung von tierischen Lebensmitteln auf Chlorkohlenwasserstoffe
- Der Einsatz der automatischen Gelchromatographie zur Reinigung von Pesticidextrakten Organochlor
- Pflanzenbehandlungsmittel in Tabak und Tabakerzeugnissen
- Bestimmung der Fungizide Bitertanol, Fuberidazol, Imazalil, Rabenzazole, Triadimefon und Triadimenol in Pflanzen und Boden
- Methode zur Aufarbeitung von Lebensmitteln und Futtermitteln pflanzlicher und tierischer Herkunft für die Multirückstandsbestimmung lipoid- und wasserlöslicher Pflanzenbehandlungsmittel
- Zur Analytik von Chlorkohlenwasserstoffen in Zwiebeln nach Reinigung mit der Gelpermeationschromatographie
- Schnelle Untersuchung von Milch auf chlorierte Kohlenwasserstoffe mittels automatischer Gelchromatographie
- Automatisierte Gelchromatographie als Reinigungsverfahren zum Nachweis von ECD-erfaßbaren Wirkstoffen, chlorierten Kohlenwasserstoffen, Pentachlorphenol sowie von Diphenyl und o-Phenylphenol in pflanzlichen Materialien
- Untersuchungen zum Einsatz der Gelpermeationschromatograpie in der Rückstandsanalytik
- Nachweis von Aflatoxin B1 in Futtermitteln für Milchtiere
- Bestimmung der Rückstände von aromatischen Dinitroverbindungen mittels gelchromatischer Reinigung
- Die Gelpermeationschromatographie, eine universelle Reinigungsmethode in der Analytik von Pflanzenschutzmitteln
- Untersuchungen zur Messung und Bewertung von Rückständen des Ektoparasitenbekämpfungsmittels Phoxim in Milch
- Methode zur Aufarbeitung von Lebensmitteln und Futtermitteln pflanzlicher und tierischer Herkunft für die
- Multirückstandsbestimmung lipoid- und wasserlöslicher Pflanzenbehandlungsmittel
- Untersuchungen zur Gelchromatograpie (GPC) als Reinigungsverfahren in der Rückstandsanalytik von Tierarzneimitteln
- Eine schnelle Methode zur Bestimmung des Ebergeruchsteroids Androstenon
- Analysenverfahren zur Bestimmung von polychlorierten Dibenzodioxinen und Dibenzofuranen in Frauenmilch
- Untersuchungen zum Vorkommen von Moschus-Xylol in Fischen
- GPC-clean up von fetthaltigen Matrizes in der Rückstandsanalytik unter Verwendung von OPTIMA-Säulen
- Entwicklung einer Methode zur Bestimmung von Nitromoschusverbindungen im Hausstaub
Produktanfrage
Gerne beraten wir Sie zu unseren Systemen auch persönlich und beantworten Ihre Fragen. Wir sind für Sie telefonisch erreichbar und stellen Ihnen ein Kontaktformular zur Verfügung. Wir freuen uns auf Ihre Anfrage und melden uns bei Ihnen so bald wie möglich.
Kontakt
Zentrale
ANTEC GmbH
Analysen- und Prozesstechnik
Hauptstraße 4
82404 Sindelsdorf
Telefon: +49 (0) 8856 9910
E-Mail: kontakt@antec.de